 Yrd. Doç. Dr. Murat DOĞAN
Yrd. Doç. Dr. Murat DOĞAN
Telomerler kromozomların uç bölgelerinde bulunan DNA ve proteinlerdir. Kromozomların her iki kolunun sonunda bulunur ve genom stabilitesini sağlarlar. Yapısal ve fonksiyonel olarak diğer kromozomal DNA dizilerinden farklı olan telomerlerin sentezinden telomeraz enzimi sorumludur.
Telomerlerin uç bölgelerde bulunmasının nedeni iki problemi çözmek amaçlıdır. Bu problemlerden ilki kromozom uçlarının replikasyonlarının tamamlanmasını sağlamak, ikinci problem ise bu uçların birbirleri ile karışmasını ya da kromozomların iç kısımları ile reaksiyon vermelerini önlemektir. Telomeraz enzimi sayesinde sentezlenen telomerler kromozomların uç bölgelerinin korunması için büyük önem teşkil eder. Uç bölgelerde telomerlerin olmaması durumunda kromozomların daha kararsız ve dayanıksız olduğu kanıtlanmıştır.
1960’lı yıllara kadar hücrelerin sınırsız büyüme yeteneklerinin olduğu düşünülüyordu. Yapılan araştırmalar gösterdi ki hücrelerin belirli bir bölünme sayısı vardır ve bu sınırlı bölünmenin maksimum değerine Hayflick limiti denir. Hayflick limitine ulaşan hücreler bölünmeden uzaklaşarak morfolojik ve biyokimyasal değişiklikler yaşayarak replikatif yaşlanma dönemine geçiş sağlarlar. Hücrenin replikatif yaşlanmaya geçişinde Hayflick limitine ulaşmak için telomerlerin etkisi olduğu çalışmalarla desteklenmektedir. Kromozomlarda bulunan telomerik tekrarların uzunluğu bölünmeler sonrasında değişebilir. Hücre kültüründeki ölü hücrelere ait telomerlerin birinci nesil başına 65 baz çifti (bp) kadar kısaldığı çalışmalarda bildirilmektedir.
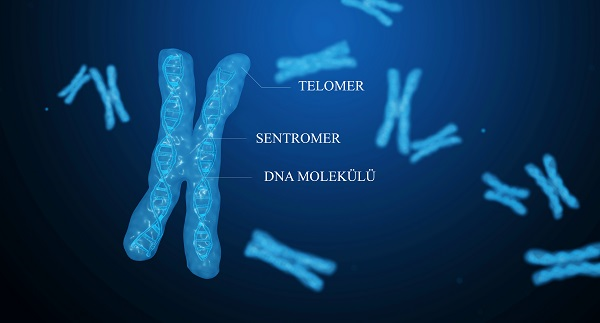
İnsana ait üreme dizisi hücrelerinin kromozomal uçlarında 10 kb’lık telomerik AGGGTT tekrarları vardır. Telomer uzunluğu ile yaş arasındaki ilişkiyi aydınlatmak amacı ile farklı yaşlardaki insanlara ait hücrelerde, insan fibroblastlarının ön kültürlerinde ve bazı kanser hücrelerinde çalışmalar yapılmıştır. Bu çalışmaların sonucunda telomer uzunluğunun artan hücre bölünme hızı veya yaşı ile azaldığı anlaşılmıştır. 1973 yılında Olovnikov’un yaptığı çalışmada telomer kısalmasının ileride ölüme yol açabileceğini, somatik hücrelerde çoğalmayı sınırlayıp hücre yaşlanmasına neden olabileceğini bildirmiştir. Normal dokulardaki telomerin uzatılmasından görevli olan sistemler, bölünme olduğu süreçte etkinliklerini sürdürmezler. Bu nedenle telomerler hücre bölünmesi sırasında kısalırlar. Telomer uzunluğu hücrelerin replikatif yaşama süresini belirlerler ve Telomerler kritik uzunluğa kadar kısaldıklarında yaşlanma programı aktive olur. Bundan sonra hücre bölünmesi durur. Fakat yaşamaya ve fonksiyonlarına devam ederler.
Eşey hücrelerinde telomerlerin bakımı aktif olarak yapılmaktadır. Eşey hücrelerinin yavru hücrelere uzunluğunu kaybetmemiş kromozomları transfer etmek zorundadırlar. Fakat telomer hipotezi somatik dokularda yaşlanma ile telomer uzunluğunun azaldığını ileri sürmektedir. Sperm hücreleri uzun telomer dizilerine sahiptir ve telomer uzunluğu korunmaktadır. Buna karşın kan hücrelerinde telomer uzunluğunun yaşlanma ile azaldığı anlaşılmıştır. Bu sonuçlar, eşey hücrelerinin telomer bütünlüğünü sağladığını fakat somatik dokuların bunu yapamadıklarını göstermektedir.
Telomer-Telomeraz aktivitesinin insanlarda birçok hastalığın patolojisi ve immun fonksiyonlarıyla da ilişkili olduğu çalışmalarda gösterilmiştir. Telomeraz aktivitesinin artışının yaşlanma etkilerini azaltabileceği çalışmalarla desteklenmektedir. Telomeraz aktivitesini artırıcı doğal tedavi seçenekleri bulunmaktadır. Bunlar Gingko Biloba, B vitaminleri, D vitamini, Resveratrol, Kurkumin, Sikloastragenol, E vitamini ve C vitamini de telomeraz aktivitesini koruyucu ve arttırıcı etki göstermektedir. Bu sayede yaşlanmanın etkilerinin azalması muhtemeldir.

KAYNAKÇA